二、主要法规
MEDICAL DEVICE ACT 2012(LAWS OF MALAYSIA Act 737)
< 2012年《医疗器械法》(第 737 号法案)(附件2.1)>
MEDICAL DEVICE AUTHORITY ACT 2012(LAWS OF MALAYSIA Act 738)
< 2012年《医疗器械管理局法》(第 738 号法案)(附件2.2)>
三、马来西亚医疗器械市场准入的注册流程
HOW TO APPLY FOR MEDICAL DEVICE REGISTRATION UNDER MEDICAL DEVICE ACT 2012 (ACT 737)
< 依据2012年《医疗器械法》(第 737 号法案)进行医疗器械注册申请指南(附件 2.3)>
所有在马来西亚生产、进口的医疗器械产品都必须在医疗器械管理局进行注册后方可进入市场。
注册申报系统为MDA医疗器械注册系统:Medical Device Centralized Online Application System (MeDC@St)
对于进口的医疗器械生产商而言,需找到授权代理(authorized represetative,AR)完成注册事宜及负责上市后的跟踪等事务,
授权代表必须是马来西亚公民或永久居民,并且必须持有营业执照和医疗器械良好分销规(GDPMD)证书。医疗器械注册申请将由授权代表提交,而符合性评估机构(CAB)的证书也将以授权代表的名义签发。 注册证有效期为5年。
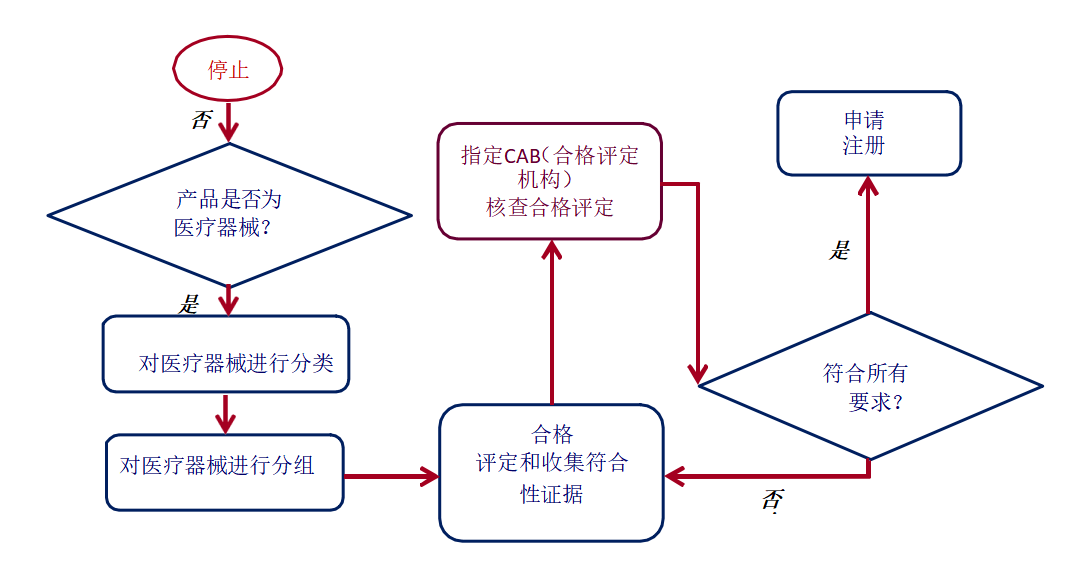
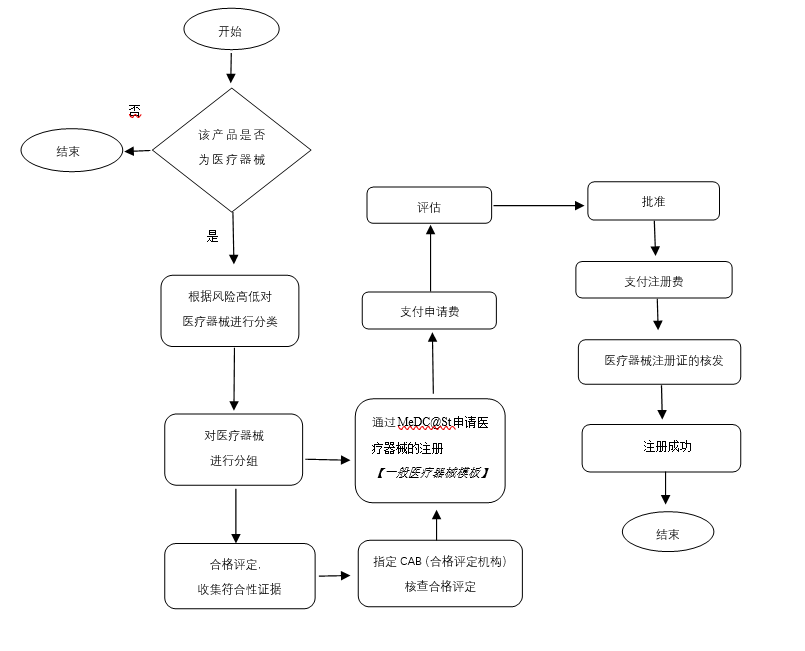
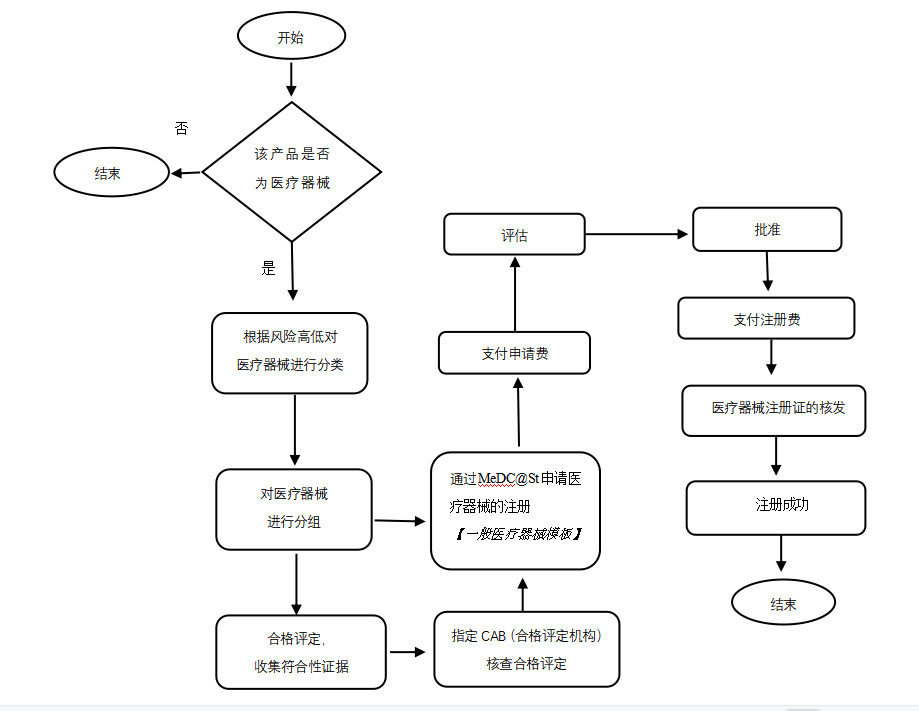
1.医疗器械注册流程概述
注册前提
A类一般医疗器械
* A类医疗器械可豁免合格评定程序。
B类、C类、D类一般医疗器械